Od dawna wiadomo, że wszystkie cząsteczki mają dwa równe i przeciwne ładunki, które są oddzielone na pewną odległość. W przypadku takich polarnych cząsteczek środek ładunku ujemnego nie pokrywa się ze środkiem ładunku dodatniego. Stopień polarności w takich kowalencyjnych cząsteczkach można opisać terminem dipolowym, który jest zasadniczo miarą polarności w polarnym wiązaniu kowalencyjnym.
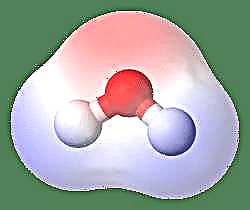
Najprostszym przykładem dipola jest cząsteczka wody. Cząsteczka wody jest polarna z powodu nierównego podziału jej elektronów w „zgiętej” strukturze. Cząsteczka wody tworzy kąt z atomami wodoru na końcach i tlenem na wierzchołku. Ponieważ tlen ma wyższą elektroujemność niż wodór, strona cząsteczki z atomem tlenu ma częściowy ładunek ujemny, podczas gdy wodór w środku ma częściowy ładunek dodatni. Z tego powodu kierunek momentu dipolowego wskazuje na tlen.
W języku fizyki elektryczny moment dipolowy jest miarą rozdziału dodatnich i ujemnych ładunków elektrycznych w układzie ładunków, to znaczy miarą ogólnej polaryzacji układu ładunków - tj. Separacji ładunku elektrycznego cząsteczek, która prowadzi do dipola. Matematycznie oraz w prostym przypadku dwóch ładunków punktowych, jednego z ładunkiem + q i jednego z ładunkiem? Q, elektryczny dipolowy moment p można wyrazić jako: p = qd, gdzie d jest wektorem przemieszczenia wskazującym od ładunku ujemnego do ładunek dodatni. Zatem elektryczny wektor momentu dipolowego p wskazuje od ładunku ujemnego do ładunku dodatniego.
Innym sposobem spojrzenia na to jest przedstawienie momentu dipolowego grecką literą m, m = ed, gdzie e jest ładunkiem elektrycznym, a d jest odległością separacji. Jest wyrażany w jednostkach Debye i zapisywany jako D (gdzie 1 Debye = 1 x 10-18e.s.u cm). Moment dipolowy jest wielkością wektorową i dlatego jest reprezentowany przez małą strzałkę z ogonem w dodatnim środku i głową skierowaną w kierunku ujemnego środka. W przypadku cząsteczki wody moment dipolowy wynosi 1,85 D, podczas gdy cząsteczka kwasu chlorowodorowego ma 1,03 D i może być reprezentowana jako:
Napisaliśmy wiele artykułów na temat momentu dipola dla Space Magazine. Oto artykuł o tym, z czego zbudowana jest woda, a tutaj artykuł o cząsteczkach.
Jeśli chcesz uzyskać więcej informacji na temat momentu dipola, sprawdź te artykuły w Hyperphysics and Science Daily.
Nagraliśmy również cały odcinek Astronomy Cast All about Molecules in Space. Posłuchaj tutaj, odcinek 116: Molekuły w kosmosie.
Źródła:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule